Los productos finales de glicación avanzada (AGEs) han ganado fama como “enemigos silenciosos” en la dieta, vinculados a inflamación, envejecimiento acelerado y enfermedades crónicas. El razonamiento es atractivo: se forman cuando proteínas y azúcares reaccionan (reacción de Maillard, la misma que dora un pan o un filete) y, si los comemos, podrían acumularse en nuestros tejidos y dañar nuestras células. Pero como suele pasar en nutrición, la historia es más compleja, sobre todo cuando pasamos de modelos mecanísticos y en animales a lo que realmente ocurre en humanos. Con la modernización de la alimentación y el uso extendido de técnicas culinarias como horneado, fritura, parrilla y asado a alta temperatura, la exposición dietaria a AGEs ha aumentado sustancialmente en comparación con patrones tradicionales de cocción más suaves. Alimentos ricos en proteína y grasa animal, sometidos a calor seco, concentran gran parte de estos compuestos. Esta realidad ha motivado a la comunidad científica a preguntarse si los AGEs exógenos representan un riesgo relevante para la salud, o si su impacto es marginal frente a otros determinantes dietarios y metabólicos. Y, por supuesto, no faltan los “eruditos” que advierten con solemnidad que “si cocinas tu proteína en polvo la destruyes y te intoxicas de químicos”, como si un par de hot cakes proteicos fueran la puerta de entrada a un apocalipsis glicado.
¿Qué son los AGEs y por qué se habla tanto de la CML?
Dentro del gran grupo de AGEs, la Nε-(carboximetil)lisina (CML) es de las más estudiadas. Se forma tanto endógenamente (en tu propio cuerpo, especialmente con hiperglucemia, estrés oxidativo o envejecimiento) como exógenamente (en alimentos muy procesados, cocciones a alta temperatura o tabaquismo). En laboratorio, la CML unida a proteínas puede interactuar con receptores como RAGE (receptor de AGEs), activando vías proinflamatorias. La CML libre, en cambio, se elimina rápido por orina y no parece tener la misma capacidad de activar RAGE.
El CML es protagonista en la investigación porque:
- Es uno de los AGEs más abundantes en alimentos y tejidos humanos.
- Se detecta con métodos validados (ELISA, LC-MS/MS, marcaje isotópico).
- Está presente tanto en forma libre como unida a proteínas, lo que permite estudiar procesos rápidos y acumulativos.
- El CML unido a proteínas tiene relevancia fisiopatológica por su interacción con RAGE.
- La mayoría de los estudios experimentales y clínicos utilizan CML como marcador de exposición a AGEs.
Por eso, no es lo mismo medir la CML libre en plasma u orina —que refleja cambios recientes en la dieta— que la CML unida a proteínas en tejidos, que indica acumulación a más largo plazo y podría tener mayor relevancia biológica.
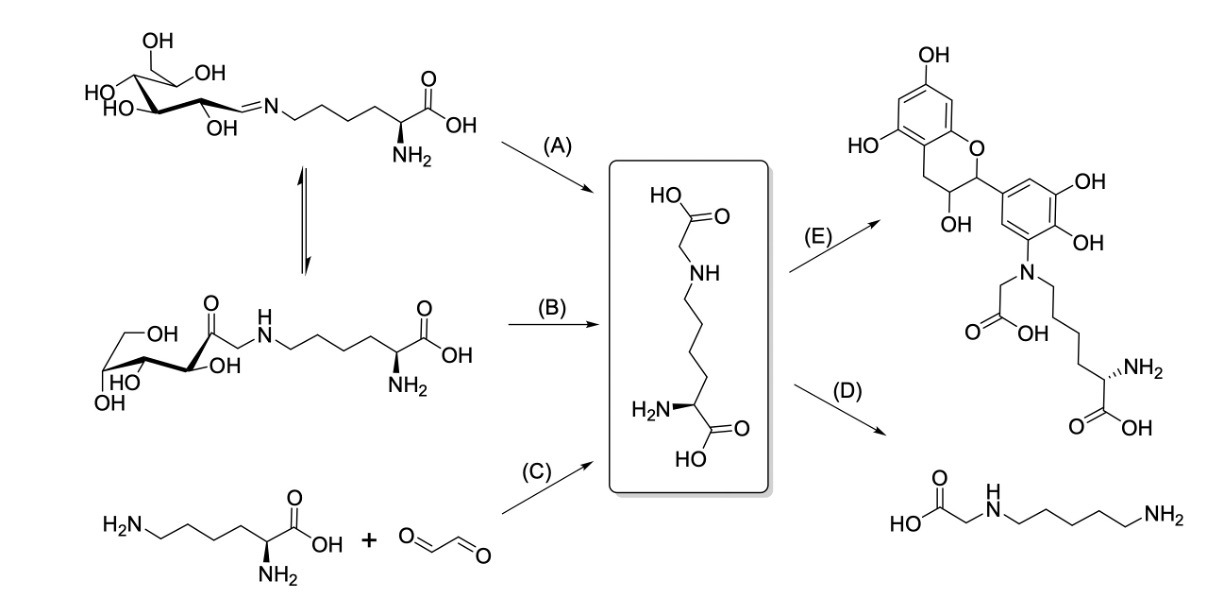
Si quieres entrar en la parte más técnica, aquí va la versión completa: la Nε-(carboximetil)lisina (CML) es uno de los compuestos más característicos que aparecen en las etapas avanzadas de la reacción de Maillard. Todo inicia cuando un azúcar reductor entra en contacto con el grupo ε-amino de la lisina presente en una proteína. Este primer encuentro da lugar a una base de Schiff inestable, que rápidamente se reorganiza formando un producto de Amadori. A partir de ahí, la historia química se complica: ese producto intermedio puede oxidarse, bien desde la propia base de Schiff, bien desde el Amadori, o el grupo ε-amino de la lisina puede reaccionar directamente con glicoxal, un compuesto altamente reactivo que puede originarse tanto de la glicación como de la peroxidación lipídica. Cualquiera de estas rutas culmina con la adición irreversible de un grupo carboximetilo a la lisina, sellando así su transformación en CML . En resumen, hablamos de un cambio químico estable, capaz de acumularse en tejidos y servir como marcador de glicación avanzada.
Imagen 2. Cómo nace la CML: de un dulce encuentro a una unión irreversible
Evidencia en modelos animales: dosis, hallazgos y limitaciones
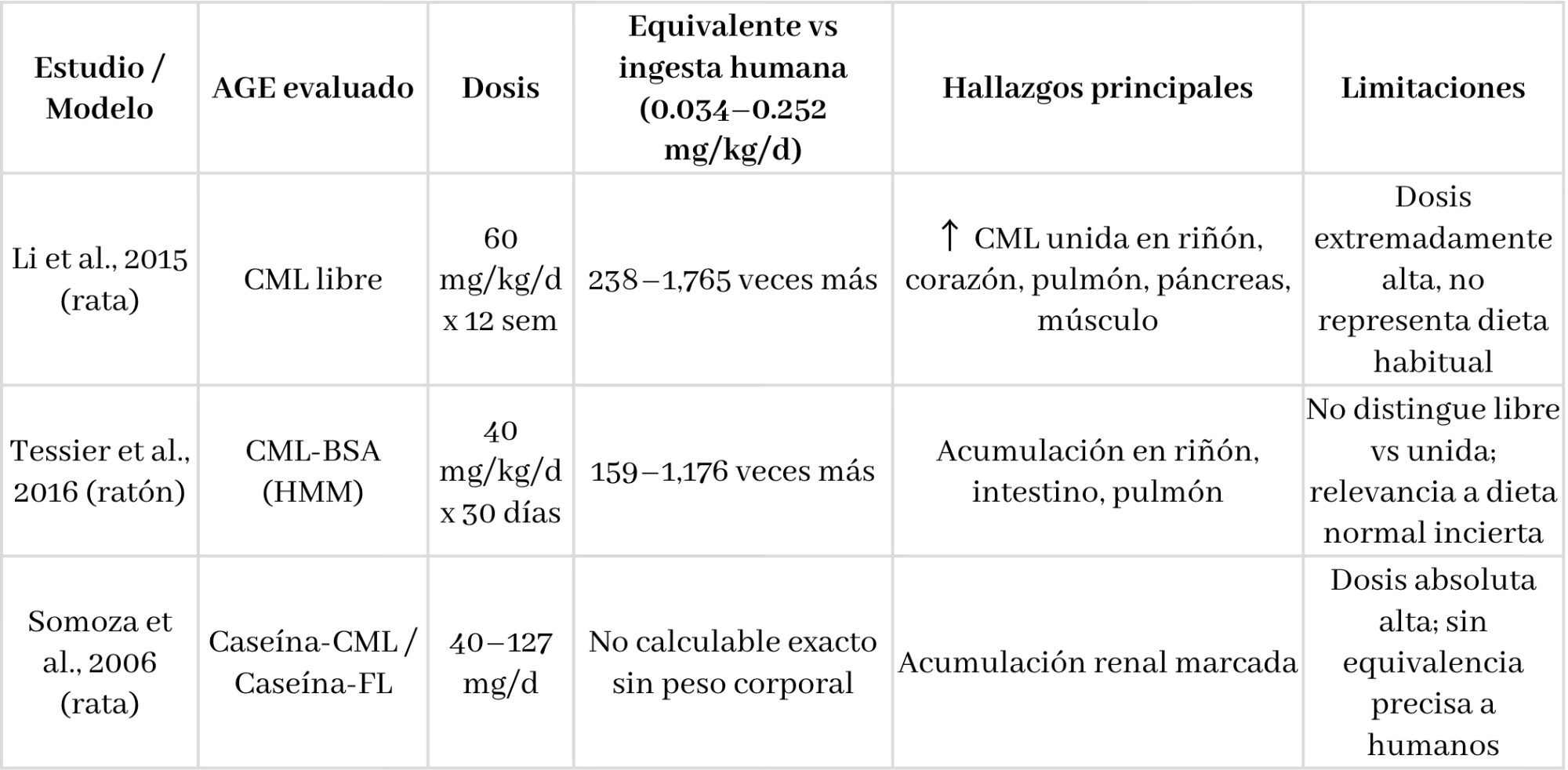
En animales, se han usado dosis de AGEs y CML cientos o miles de veces mayores a la ingesta humana promedio para “forzar” una respuesta y así estudiar su distribución y efectos (tabla 1). Esto permite mapear mecanismos, pero también plantea un problema obvio: la extrapolación directa a la vida real es muy arriesgada. Una buena forma de ponerlo en perspectiva es imaginar que evaluamos los efectos del agua —algo considerado “saludable”—, pero administrando 2 o 3 órdenes de magnitud más de lo habitual: no serían 2 litros al día, sino 100 o hasta 1000 litros en una sola jornada, algo incompatible con la vida. La hormesis, el principio de que la dosis define el efecto, también aplica aquí. Y si pensamos en una sustancia nociva como el tabaco, el exceso sería igual de desmesurado: no sería fumar un cigarro ocasional, sino 100 al día, o incluso 100 cajetillas diarias. Este contraste ayuda a entender por qué los hallazgos de acumulación y daño en modelos animales con dosis extremas no se pueden trasladar de forma directa a la dieta humana habitual.
Tabla 1. Evidencia en modelos animales
¿Por qué se usan estas dosis tan altas?
Aceleran la aparición de cambios medibles, reduciendo el tiempo necesario para observar efectos.
Facilitan rastrear la distribución en tejidos y estudiar con mayor claridad los mecanismos de interacción del compuesto.
¿Por qué esto limita la extrapolación?
El metabolismo y la absorción no son lineales: lo que ocurre con dosis masivas no refleja lo que sucede con dosis dietarias.
Los efectos observados pueden deberse más a una sobrecarga metabólica que a la acción intrínseca del compuesto.
Evidencia directa en humanos: lo que sabemos y lo que no
En humanos, los estudios sobre AGEs —incluyendo CML— suelen evaluar formas libres de baja masa molecular (BMM) y formas unidas a proteínas de alta masa molecular (AMM). Esta distinción es relevante porque los AGEs HMM tienden a absorberse menos en el tracto digestivo y su detección en circulación probablemente provenga más de producción endógena que de absorción directa. Por el contrario, los AGEs LMM pueden absorberse con mayor facilidad, circular libremente y eliminarse más rápido por orina. Además, una fracción de los AGEs o de sus precursores reactivos puede ser neutralizada o degradada antes de la absorción por enzimas, antioxidantes, microorganismos o reacciones químicas en el tracto digestivo, lo que reduciría su biodisponibilidad.
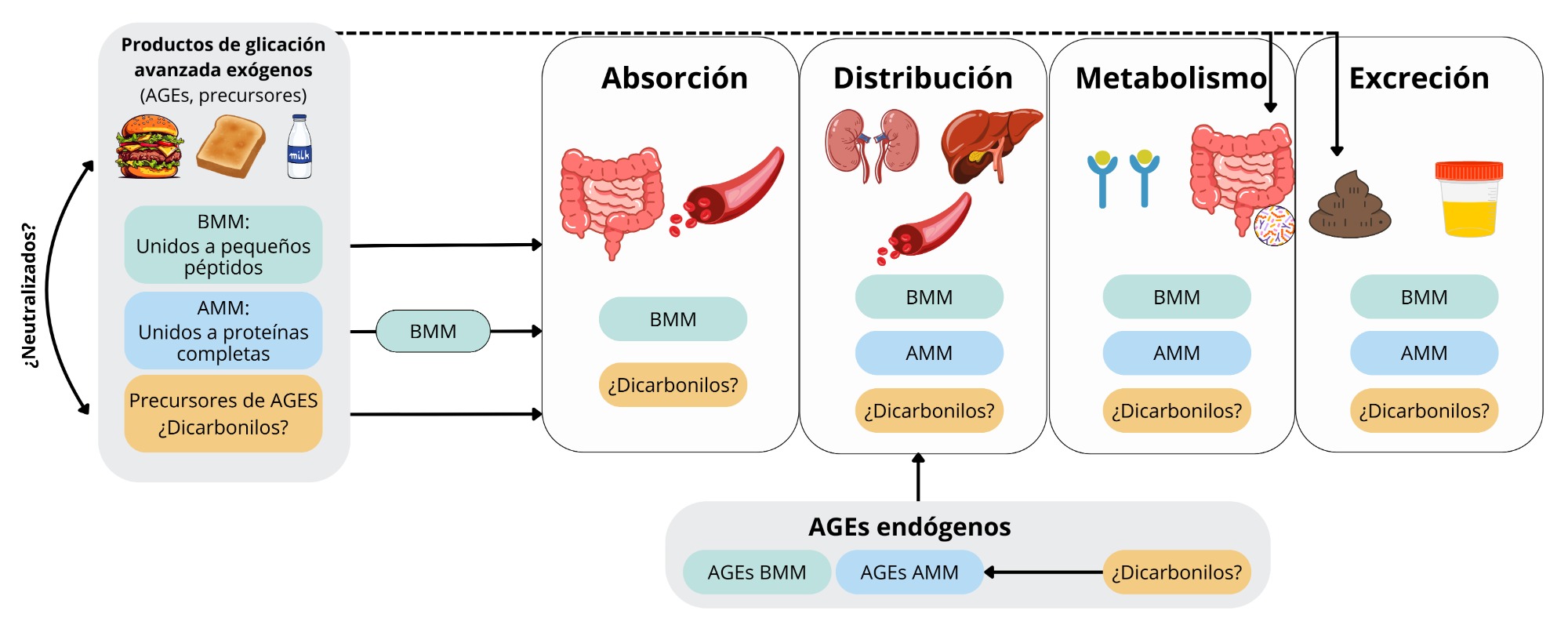
Esta dinámica condiciona la interpretación de resultados (imagen 1):
Predominio en heces → sugiere escasa absorción intestinal o eliminación directa sin metabolizar. En el caso de precursores reactivos, también podría indicar que reaccionaron localmente antes de ser absorbidos.
Aumento en orina → indica absorción y eliminación rápida; en precursores, podría reflejar excreción directa o metabolización a AGEs más pequeños y solubles.
Aumento en sangre pero no en orina → puede reflejar retención en tejidos (en el caso de AGEs HMM o de AGEs recién formados a partir de precursores).
Imagen 1. Factores que influyen en la disponibilidad de los compuestos de glicación avanzada.
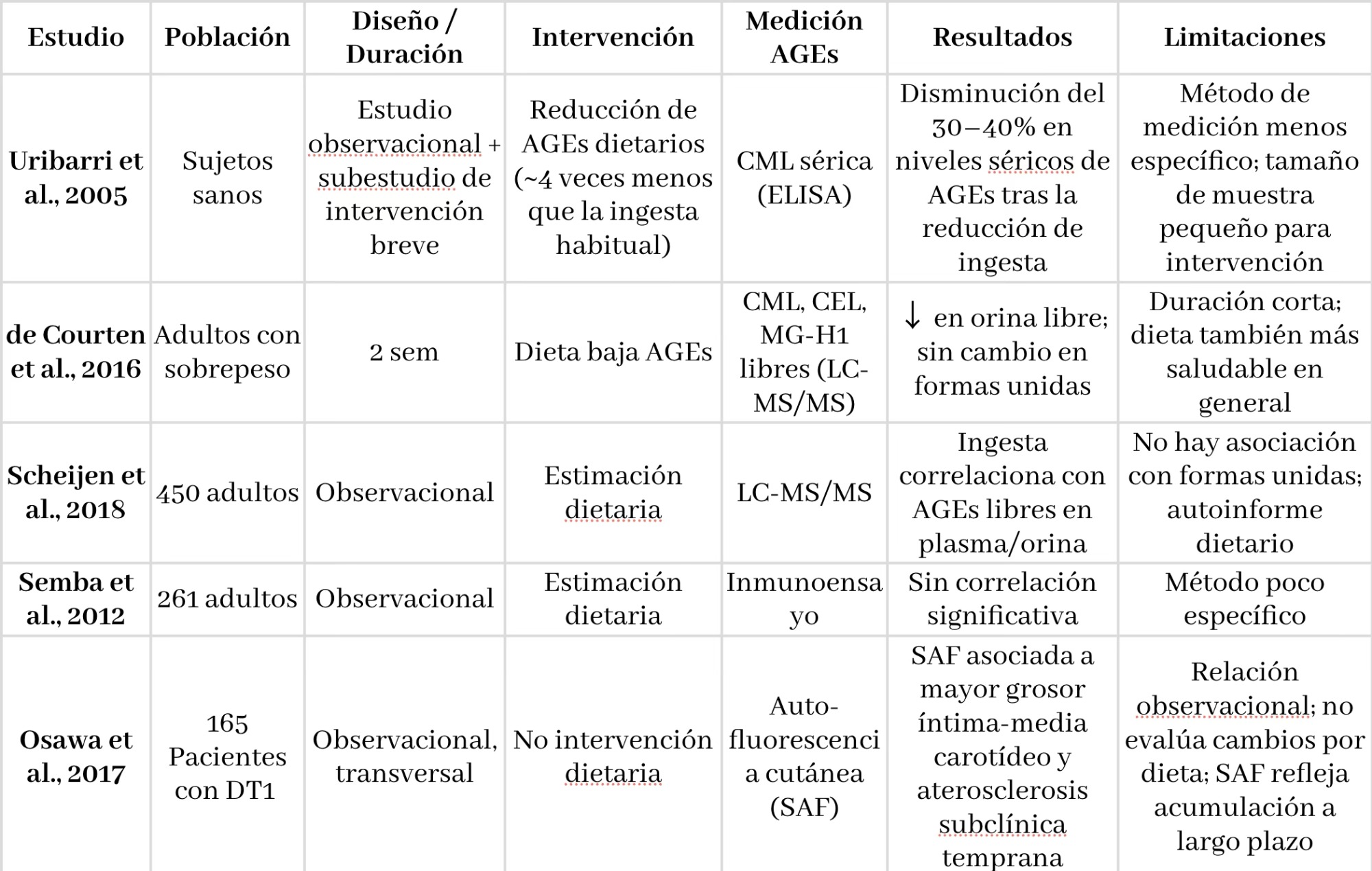
En humanos sí hay estudios que miden el impacto de reducir AGEs dietarios (tabla 2), pero casi todos son cortos, usan marcadores intermedios y no desenlaces clínicos a largo plazo. Un aspecto relevante de la investigación reciente es la medición no invasiva de AGEs tisulares mediante autofluorescencia cutánea (SAF), que estima la acumulación en proteínas de larga vida como el colágeno dérmico. La SAF se correlaciona con la edad, la diabetes y la enfermedad renal crónica, pero en ensayos de corta duración con dietas bajas en AGEs no se han observado cambios significativos, lo que sugiere que la fracción tisular de AGEs se modifica lentamente y requiere meses o años para mostrar cambios medibles. En contraste, la fracción libre circulante puede responder en cuestión de semanas.
Tabla 2. Evidencia relevante en humanos.
Factores que influyen en la disponibilidad de AGEs:
Como se mencionó anteriormente, la cantidad de AGEs detectada en heces o en circulación está modulada por múltiples factores. A lo ya señalado, se suman la composición de la matriz alimentaria (fibra, antioxidantes), el estado de la microbiota intestinal, la integridad de la mucosa, y condiciones clínicas como diabetes o enfermedad renal crónica, que pueden modificar la absorción y la capacidad de eliminación. En particular, los AGEs unidos a proteínas (HMM) tienen baja absorción intestinal y se excretan mayormente por heces, lo que ayuda a explicar por qué la relación entre ingesta estimada y niveles circulantes o tisulares no siempre es lineal.
Puntos críticos al interpretar:
Casi siempre, la dieta baja en AGEs también es más baja en ultraprocesados, calorías y azúcares → imposible saber si el cambio en AGEs libres se debe solo a los AGEs exógenos.
Este tipo de dietas suele incluir más frutas, verduras, legumbres y cereales integrales, así como menos carnes procesadas, frituras y alimentos preparados a alta temperatura. Estos cambios globales, por sí mismos, mejoran marcadores de inflamación, estrés oxidativo, perfil lipídico y control glucémico, por lo que es poco probable que los beneficios observados se deban exclusivamente a la reducción de AGEs exógenos.
Sin trazadores isotópicos doblemente marcados, es difícil separar la contribución exógena vs endógena. Estos marcadores se han usado en investigación (por ejemplo, CML marcada con ^13C en modelos animales) para rastrear absorción y acumulación, pero su uso en humanos es muy limitado debido a costos, logística y requerimientos éticos.
Las formas libres responden rápido a la dieta; las unidas a proteínas son más estables y probablemente más relevantes para efectos biológicos.
Lo que aún falta: estudios longitudinales y desenlaces clínicos
Hasta ahora, no existen estudios de gran duración (varios años) que demuestren, de manera directa, que reducir el consumo de AGEs en la dieta, manteniendo controlados —al menos en cierta magnitud— los demás factores de estilo de vida y alimentación, prevenga eventos mayores como infartos, insuficiencia renal o muerte.
La plausibilidad biológica es alta: sabemos que la acumulación de AGEs —especialmente los que se producen dentro del cuerpo por hiperglucemia, estrés oxidativo y envejecimiento— puede contribuir a procesos de inflamación crónica y daño en órganos. Sin embargo, la fracción que proviene de los alimentos en una dieta variada y equilibrada probablemente tenga un impacto mucho menor que la producción interna, sobre todo en personas sanas.
Existen estudios observacionales que intentan ajustar estadísticamente múltiples variables para aislar el efecto de los AGEs dietarios, pero es imposible eliminar por completo el sesgo: siempre hay factores no medidos o mal cuantificados que pueden distorsionar la relación observada. Por eso, para confirmar que reducir su ingesta mejora la salud a largo plazo, se necesitarían estudios controlados y prolongados, que sigan a las personas durante años y comparen grupos con dietas lo más similares posible salvo por el contenido de AGEs.
En otras palabras: sabemos lo suficiente para tener cuidado, pero no para dar por hecho que reducir AGEs en la dieta, por sí solo, cambie el destino de una enfermedad.
Precauciones al dar recomendaciones
Cuando hablamos de AGEs en la dieta, es importante no aislar el problema de todo lo demás. Reducir la ingesta de estos compuestos no garantiza por sí solo beneficios clínicos relevantes si el resto de la alimentación y el estilo de vida se mantienen igual. Una persona puede disminuir AGEs dejando de comer ciertos alimentos, pero si sigue con una dieta pobre en frutas, verduras, fibra y proteínas de calidad, o con exceso de azúcares y grasas de mala calidad, es poco probable que vea mejoras significativas en su salud.
También conviene evitar el alarmismo. En personas con una alimentación equilibrada, rica en alimentos frescos y mínimamente procesados, la contribución de los AGEs provenientes de la dieta suele ser relativamente pequeña frente a la producción interna, sobre todo si no existen enfermedades crónicas que alteren su eliminación. Demonizar un “pan tostado” ocasional o una carne a la parrilla en el contexto de una dieta globalmente saludable no solo carece de sustento sólido, sino que puede generar ansiedad innecesaria y conductas alimentarias poco sostenibles.
Por eso, la prioridad debe ser el patrón alimentario completo: variedad, predominio de alimentos frescos, control de ultraprocesados y moderación en métodos de cocción que generen más AGEs (como frituras o exposiciones prolongadas a altas temperaturas). Este enfoque es más realista y sostenible que prohibir alimentos puntuales, y se alinea mejor con la evidencia actual, que apunta a que la calidad global y la frecuencia de consumo de ultraprocesados importan mucho más que la presencia esporádica de un alimento específico.
El caso del gym rat que desayuna protein pancakes
Imagina que tu alimentación habitual está bien estructurada: abundancia de frutas, verduras, legumbres, fuentes magras de proteína, carbohidratos de buena calidad, grasas saludables y una hidratación adecuada. Si en ese contexto usas tu proteína en polvo para preparar unos pancakes dorados de vez en cuando, el impacto de esos AGEs extra será insignificante frente a la cantidad que tu propio cuerpo produce de forma normal cada día.
Hasta ahora, no existe evidencia sólida que indique que este uso ocasional, dentro de una dieta equilibrada, tenga un efecto clínicamente relevante en tu salud. De hecho, sería mucho más determinante que mantengas un buen control de tu glucemia, un descanso de calidad y una consistencia real en tu entrenamiento, porque son factores que influyen mucho más en la producción endógena de AGEs y en la salud metabólica en general.
En la práctica, la energía y el tiempo que podrías gastar preocupándote por “si dorar la proteína genera AGEs” se aprovechan mejor asegurando que tu dieta global y tus hábitos estén en orden. En otras palabras, un pancake dorado ocasional no te va a sacar de tu camino, pero descuidar tu sueño, tu recuperación o tu constancia sí podría hacerlo.
¿Cómo aplico esta información?
Construye una base sólida: el mayor escudo frente a los AGEs es una alimentación diaria compuesta por alimentos mínimamente procesados, rica en variedad de vegetales, frutas, legumbres y fuentes de proteína de calidad. Esto crea un contexto en el que la pequeña fracción de AGEs exógenos que puedas ingerir no tenga un peso relevante sobre tu salud.
Controla los grandes generadores internos: la mayoría de los AGEs que circulan en tu cuerpo no vienen de la dieta, sino de tu propia producción endógena. Factores como glucemias elevadas de forma crónica, inflamación persistente y estrés oxidativo sostenido son los que más contribuyen a esa carga. Mantener estables tus niveles de glucosa, reducir la inflamación mediante un estilo de vida activo y controlar el estrés te dará más beneficios que eliminar por completo un tipo de cocción.
Equilibra los métodos de cocción: no se trata de desterrar por completo el dorado o el gratinado, sino de alternarlos con métodos más suaves como vapor, hervido o guisado. Así puedes disfrutar del sabor y textura que aporta el dorado, sin que se convierta en tu única forma de cocinar.
Evita el exceso crónico: donde sí hay impacto es en patrones repetidos de consumo de comidas muy procesadas, frituras frecuentes o cocciones a alta temperatura de forma diaria. Esa acumulación sostenida sí eleva la carga exógena y puede sumar a otros factores de riesgo.
No te obsesiones con lo esporádico: una comida social o un antojo ocasional no son el problema. El daño real no proviene de un momento aislado, sino de un patrón que se repite sin balancear el resto de tu alimentación y hábitos.
La clave no está en vivir evitando el pan tostado, sino en tener un estilo de vida que minimice la producción interna y el exceso crónico de AGEs. Esto se logra más con constancia en hábitos que con prohibiciones absolutas.
Dig Deeper:
Kislinger T, Fu C, Huber B, Qu W, Taguchi A, Du Yan S, Hofmann M, Yan SF, Pischetsrieder M, Stern D, Schmidt AM. N(epsilon)-(carboxymethyl)lysine adducts of proteins are ligands for receptor for advanced glycation end products that activate cell signaling pathways and modulate gene expression. J Biol Chem. 1999 Oct 29;274(44):31740-9. doi: 10.1074/jbc.274.44.31740. PMID: 10531386.
Xie J, Méndez JD, Méndez-Valenzuela V, Aguilar-Hernández MM. Cellular signalling of the receptor for advanced glycation end products (RAGE). Cell Signal. 2013 Nov;25(11):2185-97. doi: 10.1016/j.cellsig.2013.06.013. Epub 2013 Jul 6. PMID: 23838007.
Qu W, Yuan X, Zhao J, Zhang Y, Hu J, Wang J, Li J. Dietary advanced glycation end products modify gut microbial composition and partially increase colon permeability in rats. Mol Nutr Food Res. 2017 Oct;61(10). doi: 10.1002/mnfr.201700118. Epub 2017 Jul 31. PMID: 28621836.
Tian Z, Chen S, Shi Y, Wang P, Wu Y, Li G. Dietary advanced glycation end products (dAGEs): An insight between modern diet and health. Food Chem. 2023 Jul 30;415:135735. doi: 10.1016/j.foodchem.2023.135735. Epub 2023 Feb 24. PMID: 36863235.
Li M, Zeng M, He Z, Zheng Z, Qin F, Tao G, Zhang S, Chen J. Effects of Long-Term Exposure to Free Nε-(Carboxymethyl)lysine on Rats Fed a High-Fat Diet. J Agric Food Chem. 2015 Dec 30;63(51):10995-1001. doi: 10.1021/acs.jafc.5b05750. Epub 2015 Dec 18. PMID: 26652688.
Tessier FJ, Niquet-Léridon C, Jacolot P, Jouquand C, Genin M, Schmidt AM, Grossin N, Boulanger E. Quantitative assessment of organ distribution of dietary protein-bound 13 C-labeled Nɛ -carboxymethyllysine after a chronic oral exposure in mice. Mol Nutr Food Res. 2016 Nov;60(11):2446-2456. doi: 10.1002/mnfr.201600140. Epub 2016 Sep 6. PMID: 27393741.
Somoza V, Wenzel E, Weiss C, Clawin-Rädecker I, Grübel N, Erbersdobler HF. Dose-dependent utilisation of casein-linked lysinoalanine, N(epsilon)-fructoselysine and N(epsilon)-carboxymethyllysine in rats. Mol Nutr Food Res. 2006 Sep;50(9):833-41. doi: 10.1002/mnfr.200600021. PMID: 16917812.
Uribarri J, Cai W, Sandu O, Peppa M, Goldberg T, Vlassara H. Diet-derived advanced glycation end products are major contributors to the body's AGE pool and induce inflammation in healthy subjects. Ann N Y Acad Sci. 2005 Jun;1043:461-6. doi: 10.1196/annals.1333.052. PMID: 16037267.
de Courten B, de Courten MP, Soldatos G, Dougherty SL, Straznicky N, Schlaich M, Sourris KC, Chand V, Scheijen JL, Kingwell BA, Cooper ME, Schalkwijk CG, Walker KZ, Forbes JM. Diet low in advanced glycation end products increases insulin sensitivity in healthy overweight individuals: a double-blind, randomized, crossover trial. Am J Clin Nutr. 2016 Jun;103(6):1426-33. doi: 10.3945/ajcn.115.125427. Epub 2016 Mar 30. PMID: 27030534.
Scheijen JLJM, Hanssen NMJ, van Greevenbroek MM, Van der Kallen CJ, Feskens EJM, Stehouwer CDA, Schalkwijk CG. Dietary intake of advanced glycation endproducts is associated with higher levels of advanced glycation endproducts in plasma and urine: The CODAM study. Clin Nutr. 2018 Jun;37(3):919-925. doi: 10.1016/j.clnu.2017.03.019. Epub 2017 Mar 23. PMID: 29381139.
Semba RD, Gebauer SK, Baer DJ, Sun K, Turner R, Silber HA, Talegawkar S, Ferrucci L, Novotny JA. Dietary intake of advanced glycation end products did not affect endothelial function and inflammation in healthy adults in a randomized controlled trial. J Nutr. 2014 Jul;144(7):1037-42. doi: 10.3945/jn.113.189480. Epub 2014 Apr 17. PMID: 24744309; PMCID: PMC4056644.
Osawa S, Katakami N, Kuroda A, Takahara M, Sakamoto F, Kawamori D, Matsuoka T, Matsuhisa M, Shimomura I. Skin Autofluorescence is Associated with Early-stage Atherosclerosis in Patients with Type 1 Diabetes. J Atheroscler Thromb. 2017 Mar 1;24(3):312-326. doi: 10.5551/jat.35592. Epub 2016 Sep 2. PMID: 27592627; PMCID: PMC5383547.



