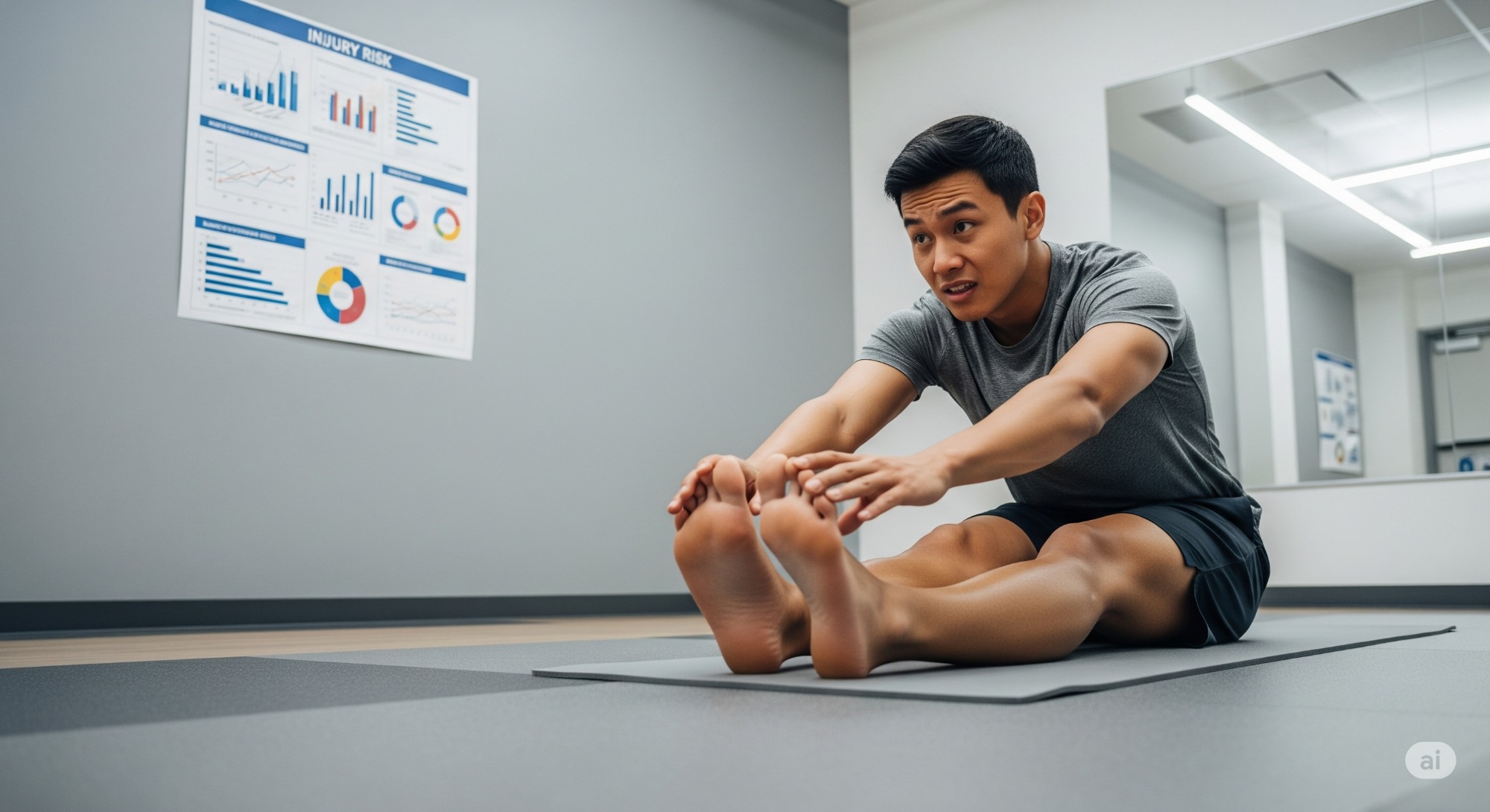
PEACE & LOVE1… seguramente ya lo has escuchado. Es un acrónimo propuesto en 2020 para el manejo de lesiones musculoesqueléticas en su fase aguda y subaguda, que rápidamente ganó popularidad entre profesionales de la salud: fisioterapeutas, médicos del deporte, entrenadores físicos, licenciados en cultura física, enfermeros deportivos, entre otros. En lo personal, confieso que su aparición me incomodó. No por su estructura, sino por la facilidad con la que muchos profesionales comenzaron a modificar su toma de decisiones clínicas, a pesar de que las recomendaciones del artículo original provenían principalmente de modelos animales y de estudios con una base limitada.
La justificación teórica de estas recomendaciones proviene en su mayoría de estudios con roedores, donde se inducía una lesión muscular de gran magnitud (mayor al 50 % del vientre muscular) y posteriormente se sometía el tejido a descensos controlados de temperatura. En ese contexto, se reportó una reducción del número de células inflamatorias, una recuperación más lenta del tejido muscular y un retraso en el retorno a la actividad. Los autores de esos trabajos sugirieron que la crioterapia, en lugar de modular la inflamación de forma adaptativa, podría estar suprimiendo esta respuesta y, con ello, entorpeciendo el proceso de reparación. Al final, vale la pena recordarlo: la inflamación existe para recuperar, no para destruir. Eliminarla completamente puede ser contraproducente.
No obstante, la evidencia en humanos ha sido siempre más confusa. Los estudios muestran una gran heterogeneidad en cuanto a los protocolos utilizados: temperatura, duración, tipo de lesión, profundidad del tejido afectado, cantidad de tejido adiposo del sujeto, momento de la intervención, entre muchas otras variables. Aun con esas limitaciones, lo mejor que teníamos disponible en ese momento sugería que la crioterapia podría tener un efecto leve o moderado para reducir el dolor, facilitar la adherencia a la rehabilitación y mejorar la experiencia del paciente durante su tratamiento2.
Durante mucho tiempo compartí literatura sobre el uso del hielo en lesiones musculares, tanto agudas como crónicas. Mi postura, entonces, fue clara: el hielo puede usarse de forma localizada después de una lesión aguda para disminuir el dolor, modular (que no suprimir) el proceso inflamatorio, y permitir trabajar más cómodamente durante la rehabilitación. Sin embargo, la evidencia evoluciona. Y mantener una postura abierta al cambio —incluso si desafía nuestras propias creencias— es parte de ejercer con responsabilidad. Hoy encuentro nueva información que me hace replantear esa postura y preguntarme, con más fundamentos: ¿qué tanto ayuda realmente el hielo en el proceso de regeneración muscular?
Un grupo de investigadores publicó recientemente un estudio que comparó los efectos de la inmersión en agua fría (IAF), termoneutral (IAT) y caliente (IAC) sobre diferentes indicadores clínicos, bioquímicos y moleculares relacionados con el dolor, el daño muscular, la inflamación y la regeneración. Y sí: vale la pena analizarlo con calma.
Vamos por pasos.
El estudio de Dablainville y colaboradores (2025) representa uno de los esfuerzos más rigurosos hasta la fecha por entender qué sucede realmente cuando aplicamos frío o calor en un músculo lesionado. Y subrayo: músculo. Porque este estudio no habla de ligamentos, ni de tendones, ni de cápsulas articulares. Habla de un solo tejido: el músculo esquelético humano.
Figura 1. Visión general del estudio
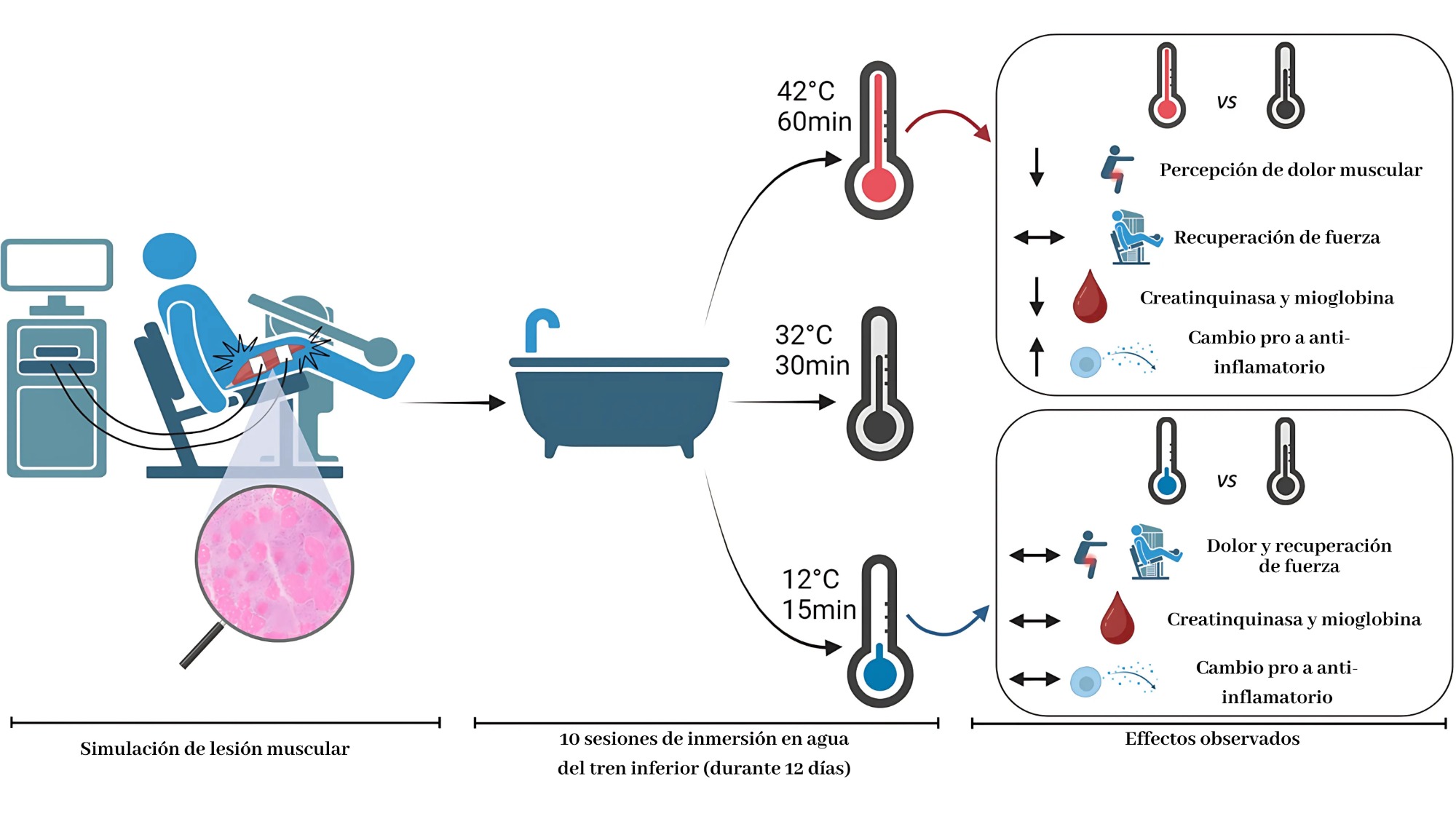
Para ello, sometieron a 34 hombres a un protocolo de daño muscular simulado: contracciones excéntricas inducidas eléctricamente sobre el cuádriceps, diseñadas para provocar necrosis de fibras musculares. A partir de ahí, dividieron a los sujetos en tres grupos que recibieron, durante 10 días consecutivos:
IAF (inmersión en agua fría, 12 °C, 15 min)
IAT (inmersión termoneutral, 32 °C, 30 min)
IAC (inmersión en agua caliente, 42 °C, 60 min)
Figura 2. Representación general de la metodología del estudio
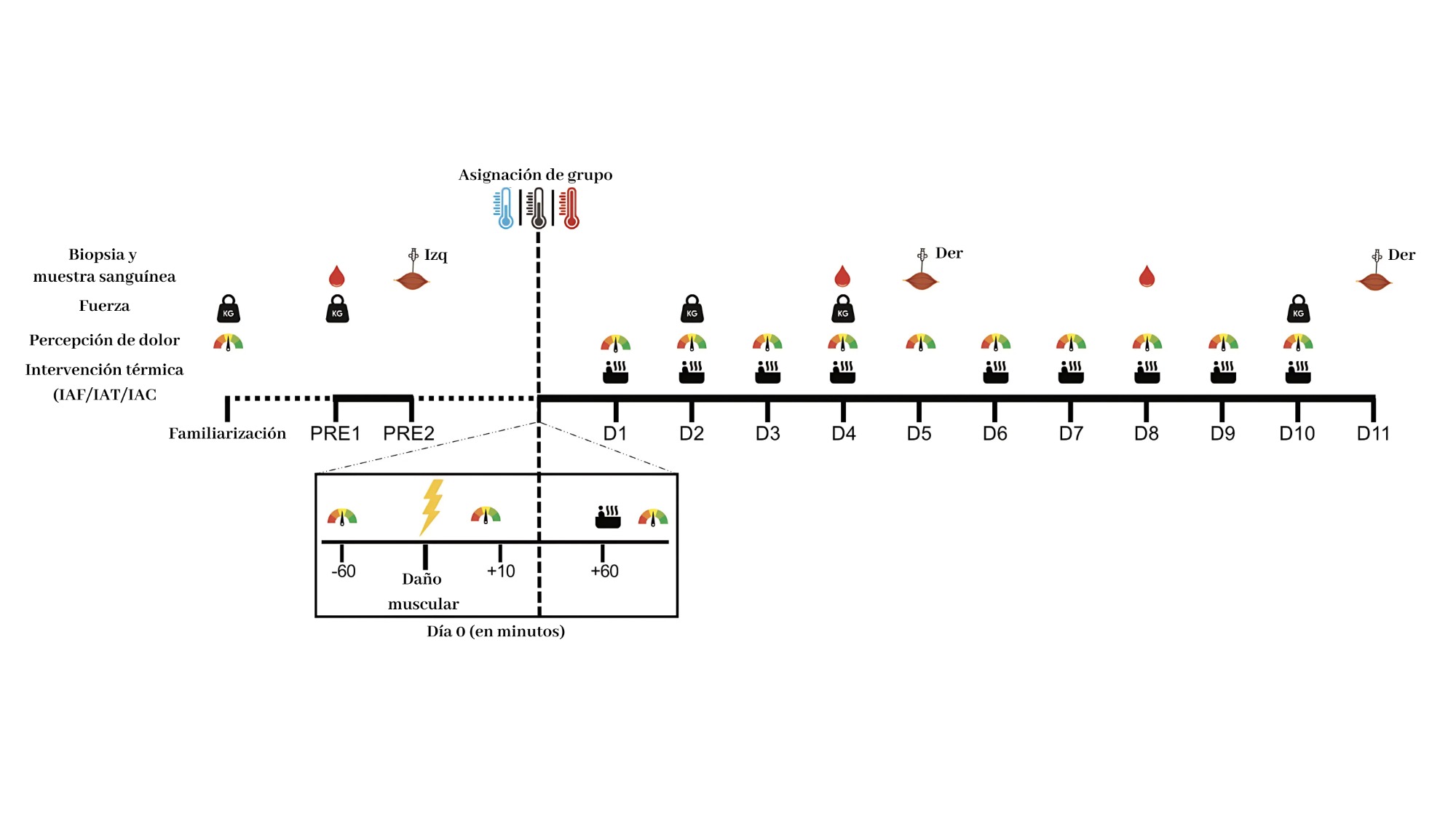
Todos los grupos recibieron su intervención una hora después de la lesión inducida, y luego cada día a la misma hora. Se midieron dolor percibido (en palpación y en sentadilla), fuerza isométrica máxima voluntaria (MVC), niveles plasmáticos de creatinquinasa (CK) y mioglobina, y se tomaron biopsias para observar la expresión de proteínas y mediadores implicados en la inflamación y regeneración muscular.
¿Qué encontraron?
Los resultados deben leerse con atención: el grupo IAC tendió a mostrar mejores respuestas en varios frentes, aunque no todas alcanzaron significancia estadística.
Dolor percibido: no hubo diferencias significativas entre grupos, pero sí una tendencia a menor dolor crónico en el grupo IAC, tanto en palpación como durante la sentadilla.
Figura 3. Representación visual del dolor percibido en los grupos de intervención
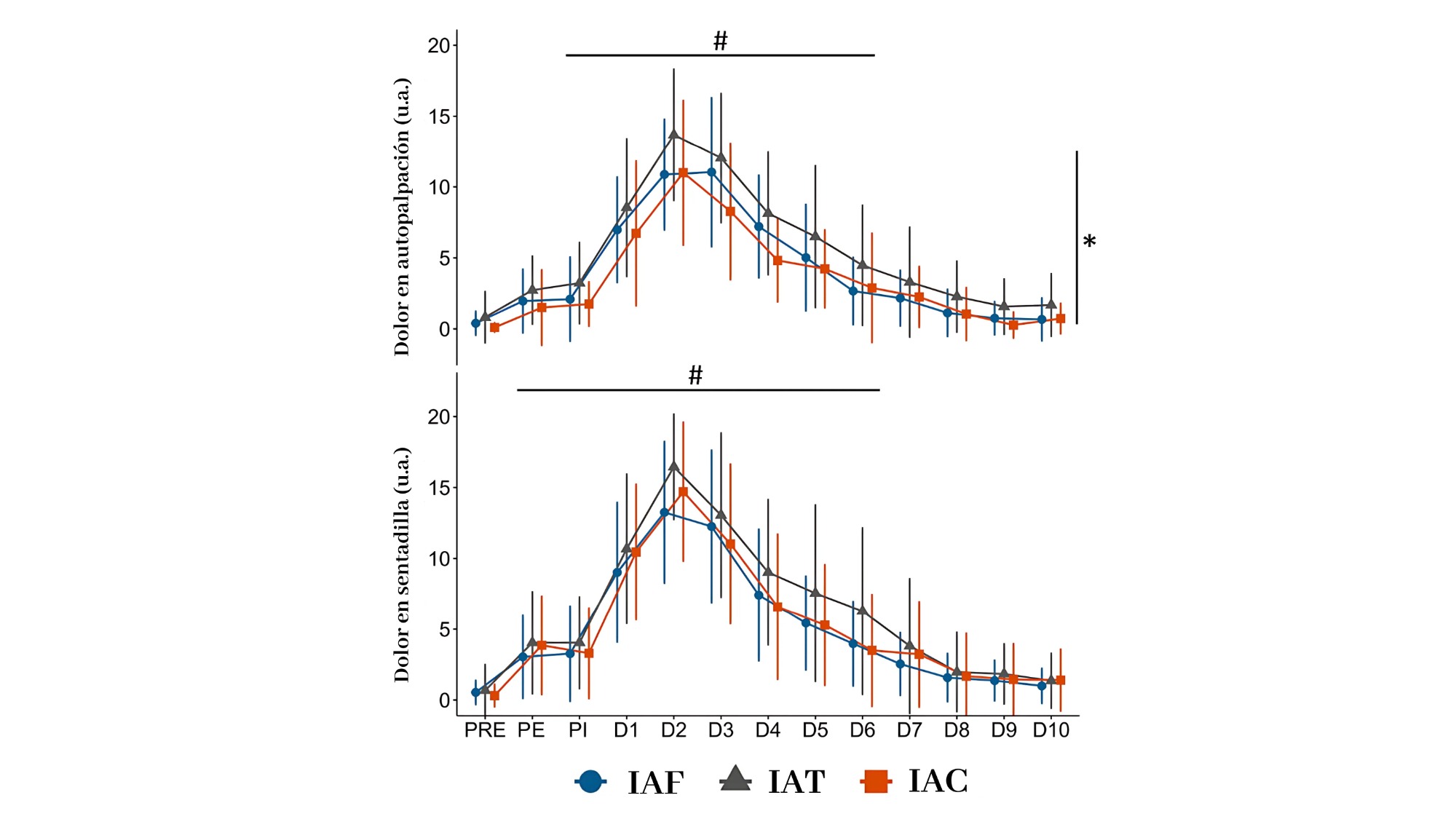
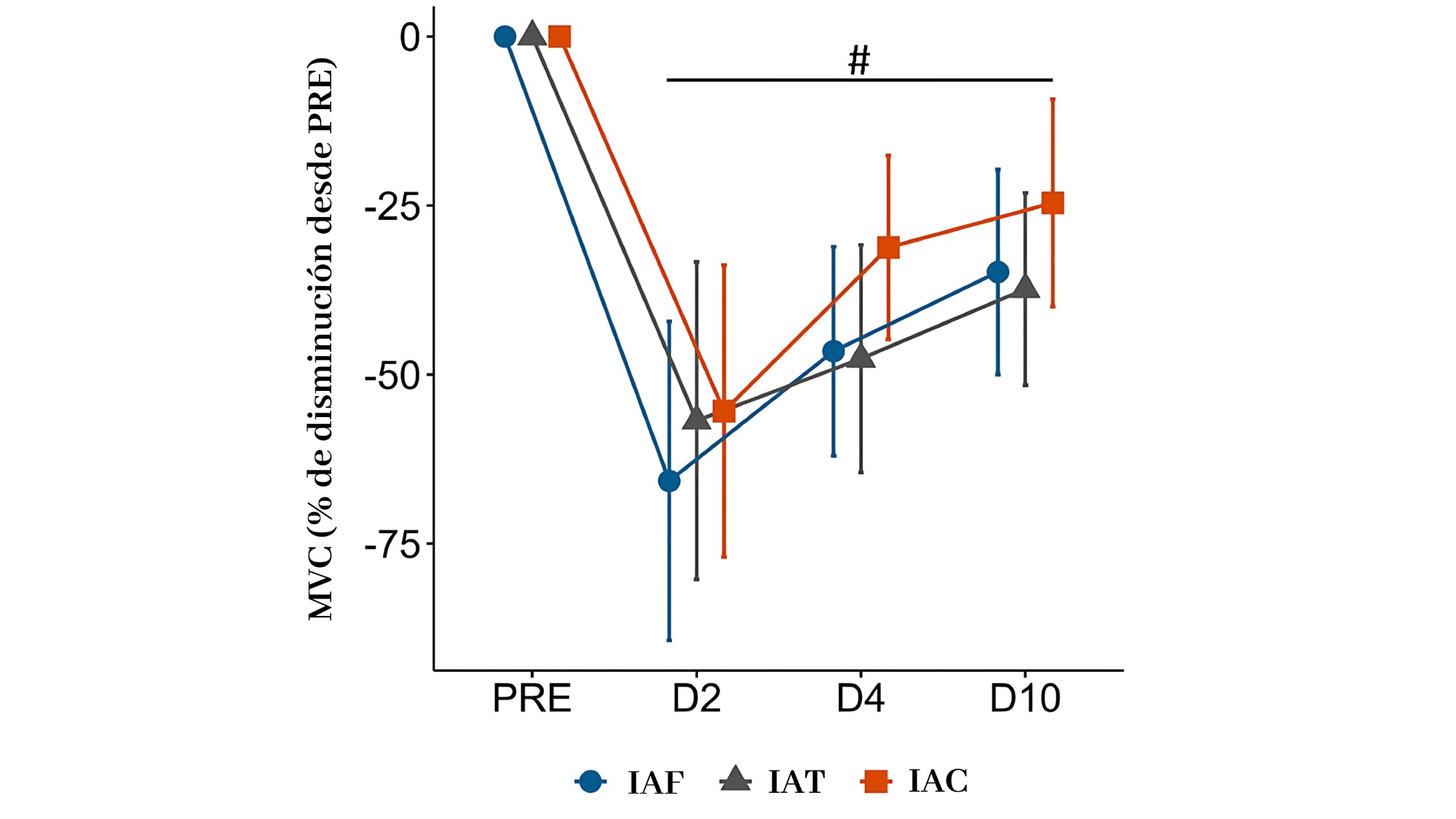
Fuerza (MVC): todos los grupos mostraron reducción postlesión y recuperación parcial a los 11 días. No hubo diferencias significativas entre grupos, pero nuevamente, la recuperación de fuerza fue numéricamente mayor en IAC.
Figura 4. Representación visual de la disminución de fuerza en los grupos de estudio.
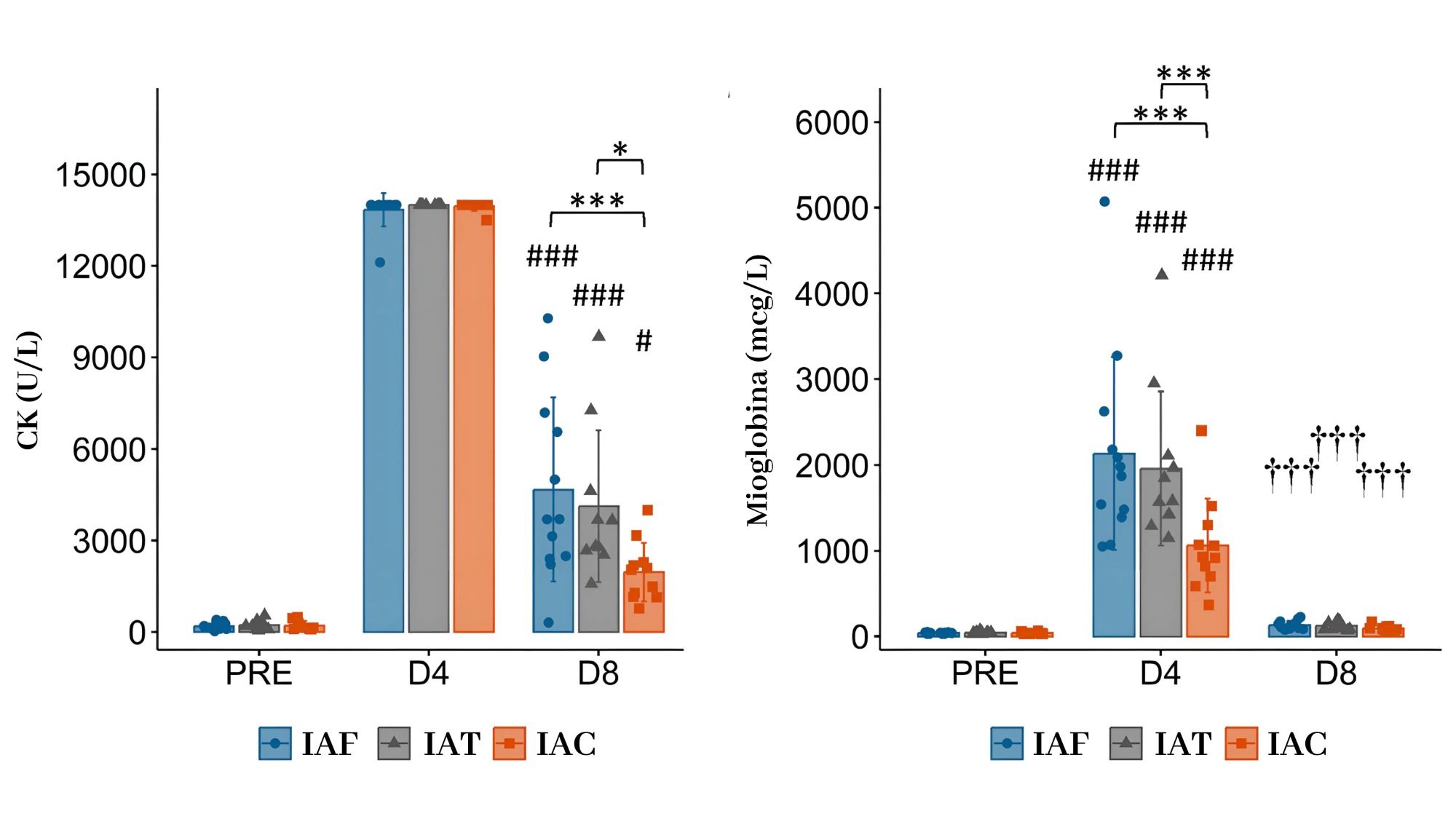
Daño muscular (CK y mioglobina): aquí sí hubo diferencias claras. IAC mostró menores concentraciones plasmáticas de CK (p ≤ 0.012) y de mioglobina (p < 0.001) en comparación con IAF e IAT. Esto sugiere una mejor contención del daño o una resolución más eficiente.
Figura 5. Representación visual de los niveles séricos de CK y mioglobina en los sujetos de estudio.
Proteínas de choque térmico (HSP27 y HSP70): IAC incrementó significativamente su expresión al día 11 (D11), mientras que IAF la atenuó. Estas proteínas son chaperonas intracelulares que participan en el plegamiento de proteínas, protección ante estrés celular y señalización regenerativa. Pero es importante decirlo: que se expresen más no garantiza una mejor regeneración. Son marcadores que sugieren un entorno celular más protegido, pero no determinan por sí solos el desenlace clínico.
NF-κB (factor nuclear kappa B): aumentó en todos los grupos, excepto en IAC. Este factor regula genes inflamatorios y catabólicos, por lo que su menor activación en IAC podría interpretarse como una señal de resolución más temprana del proceso inflamatorio.
IL-10 (interleucina-10): aumentó únicamente en IAC. Esta citocina antiinflamatoria participa en la transición hacia la fase regenerativa, y su incremento sugiere una mejor modulación del proceso inflamatorio.
Es decir, la evidencia apunta a que la IAC podría generar un entorno más favorable para la regeneración del músculo lesionado, al menos en términos de dolor, daño tisular y marcadores moleculares. Pero es fundamental remarcar que muchas de estas diferencias fueron tendencias, no hallazgos estadísticamente robustos en todos los desenlaces.
Lo que no se encontró
No se demostró que la crioterapia (IAF) mejore el dolor, la fuerza, ni la expresión de mediadores pro-regenerativos. De hecho, en varios indicadores mostró respuestas menos favorables.
Tampoco se demostró que la inmersión en agua caliente (IAC) acelere la recuperación de fuerza de forma significativa.
No se evaluaron ligamentos, tendones, ni articulaciones. El modelo está limitado al tejido muscular, y por tanto, sus hallazgos no deben extrapolarse sin cautela.
¿Qué podemos decir con todo esto?
Que la termoterapia, al menos bajo estas condiciones controladas, parece ofrecer un mejor entorno biológico para la recuperación muscular tras lesión que la crioterapia. Sin embargo, eso no implica que el calor “regenere” por sí mismo. El músculo se recupera por procesos multifactoriales: inflamación organizada, activación de células satélite, angiogénesis, síntesis proteica, entre otros. El calor parece acompañar esos procesos, quizá favoreciendo su progresión, pero no es un agente directo de reparación.
La crioterapia, por otro lado, no solo mostró efectos neutros: en algunos mediadores clave como las HSP, incluso pareció inhibir respuestas adaptativas. Esto no significa que haya que eliminar el hielo de la práctica clínica. Puede seguir siendo útil para reducir dolor agudo, facilitar adherencia a la rehabilitación o modular el edema en tejidos más superficiales. Pero como herramienta regenerativa profunda, al menos en músculo esquelético, sus beneficios siguen siendo cuestionables.
Entonces… ¿Calor o frío?
Depende. Pero si tu objetivo es promover regeneración muscular tras una lesión significativa, hoy tenemos evidencia de que el calor podría ayudar más que el frío. Eso sí, la dosis, el momento y el tipo de lesión importan. Y los efectos sobre otros tejidos (como tendones o articulaciones) pueden ser completamente distintos.
Este estudio no es una sentencia definitiva, pero sí una señal clara de que necesitamos repensar cómo, cuándo y para qué usamos las terapias térmicas. La evidencia está cambiando. Y nosotros deberíamos cambiar con ella.
Dig Deeper:
1. Dubois B, Esculier JF. Soft-tissue injuries simply need PEACE and LOVE. Br J Sports Med. 2020 Jan;54(2):72-73. doi: 10.1136/bjsports-2019-101253. Epub 2019 Aug 3 PMID: 31377722.
2. Klintberg IH, Larsson ME. Shall we use cryotherapy in the treatment in surgical procedures, in acute pain or injury, or in long term pain or dysfunction? - A systematic review. J Bodyw Mov Ther. 2021 Jul;27:368-387. doi: 10.1016/j.jbmt.2021.03.002. Epub 2021 Mar 20. PMID: 34391260.
3. Dablainville V, Mornas A, Normand-Gravier T, Al-Mulla M, Papakostas E, Olory B, Fermin TM, Zampeli F, Nader N, Alhammoud M, Bayne F, Sanchez AMJ, Cardinale M, Candau R, Bernardi H, Racinais S. Muscle regeneration is improved by hot water immersion but unchanged by cold following a simulated musculoskeletal injury in humans. J Physiol. 2025 May 28. doi: 10.1113/JP287777. Epub ahead of print. PMID: 40437768.